kovový prvok - vzácny kov, ktorý patrí do skupiny platiny. Bolo objavené v Anglicku ako výsledok experimentov s reakciou platiny. Názov osmium je uvedený v gréčtine a znamená preklad „zápach“. Čo je to ušľachtilý kov? Aké sú jeho vlastnosti a ako sa používa?

Príbeh
K objavu tohto prvku došlo náhodou v roku 1803 britskí chemici Smithson Tennant a William H. Wallastan. Výsledkom experimentov s reakciou platiny na zmes kyselín (sírovej a dusičnej) bola výsledná zrazenina nepríjemnou vôňou pripomínajúcou zápach chlóru a zhnitou reďkovkou. Podobné experimenty uskutočnili Colle Descotti, Antoine de Fourcoy a Vauclins vo Francúzsku. Výsledkom ich výskumu bolo zistenie neznámej látky v nerozpustnej zrazenine z platiny.



Neznámej látke sa potom pomenovalo pten, ale britské experimenty dokázali, že ide o dve podobné látky - irídium a osmium.
Objav týchto chemických prvkov bol predložený Kráľovskej spoločnosti v Londýne písomnou správou z Tennantu z 21. júna 1804. V periodickej tabuľke chemických prvkov je kov umiestnený pod poradovým číslom 76. Kov sa nugety nenachádza v čistej forme, preto je jeho chemický vzorec v rozpustenej forme.


Ťažba prvkov je z recyklovaných materiálov. v dôsledku jeho oddelenia od irídiovej, platinovej, platinovo-paládiovej rudy alebo medených a niklových rúd. Ročná produkcia celého prvku na svete nepresahuje veľkosť 1 tony.


záloha
Najväčšie vklady na svete stoja za povšimnutie také oblasti, ako sú Pohorie Ural a Sibír v Rusku, severnom štáte Aljaška a západný štát Kalifornia v Amerike Kanada v Severnej Amerike Kolumbia v Južnej Amerike a ďalších krajinách Juhoafrické krajiny, Austráliaostrov Tasmania, V súčasnosti sa uvažuje o významnom ložisku osmium Bushelský komplex v Južnej Afrike, dostanú tam najviac vecí. Vzhľadom na to, že najväčšie ložiská kovov sa nachádzajú v Južnej Afrike, svetové ceny tohto kovu vzácnych zemín sú dosť vysoké. Kazachstan Považuje sa za jediný hlavný vývozca osmium-187 na svete. Hoci Čína má zásoby platinovej rudy, nemá významné množstvo osmium.


Látka sa uchováva v práškovej forme a keďže sa netaví vo forme kryštálov, nie je možné ju z dôvodu jej fyzikálnych vlastností označiť. Na výrobu ingotov z tohto kovu sa používa elektrónový lúč alebo oblúkové zahrievanie z prášku, používa sa tiež zahrievanie v tégliku.


Vlastnosti
Osmium vyzerá ako strieborno-modrý kov. Je to jeden z najhustejších prvkov, jeho hustota je 22 600 kilogramov na meter kubický, ale zároveň je látka dosť krehká, ľahko sa rozpadá a rozpadá sa. Má vysokú špecifickú hmotnosť a dokáže žiariť aj pri pomerne vysokých teplotných vplyvoch. Vzhľadom na parametre a značnú teplotu topenia je ťažké ju opracovať. V prírode existuje vo forme siedmich izotopov, z ktorých šesť sa považuje za stabilné, jedná sa o osmium-184, osmium-187, osmium-188, osmium-189, osmium-190 a osmium-192. Laboratórne sa získali izotopy rádioaktívnych kovov s hmotnostnými číslami od 162 do 197 a umelo sa získali aj niektoré jadrové izoméry.
Osmium vo svojich vlastnostiach nepriaznivo ovplyvňuje všetky živé organizmy.

Takmer všetky zlúčeniny s týmto kovom spôsobujú poškodenie vnútorných orgánov, zrakové, sluchové poruchy. V prípade otravy pármi osmium sa môžu vyskytnúť ireverzibilné poruchy v tele a smrť. Vedci experimentovali na zvieratách, ktorých výsledkom bol rýchly vývoj anémie, nedostatok normálnej pľúcnej funkcie. Dospelo sa k záveru, že ide o rýchlo sa rozvíjajúci edém. Oxid osmičelý, ktorý sa používa v medicíne, je veľmi agresívna látka. Má najhoršiu vôňu na svete. Pri otrave pokožka trpí, mení farbu na zelenú alebo čiernu. Často je sprevádzaná vredmi a trhlinami, ktoré sa liečia veľmi dlho.

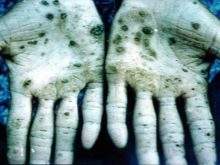

Zamestnanci priemyselných priestorov sú vystavení najvyššiemu riziku, podľa všetkých bezpečnostných noriem pracujú iba v respirátoroch a špeciálnom oblečení. Všetky nádoby obsahujúce oxid osmičelý sú zapečatené a skladované v súlade s predpismi. Na získanie minerálov Nevyanskitu sa platina premení na roztok pomocou aqua regia. Potom sa na výslednú zrazeninu pôsobí zinkom v 8-násobnom množstve - táto zliatina sa relatívne ľahko premení na práškový stav, ktorý sa potom taví s peroxidom bárnatým. Ďalším krokom je spracovanie výslednej hmoty pomocou aqua regia, destilácia cez zariadenie na separáciu oxidu osmičelého.

Vystavením látky alkalickému roztoku sa získa soľ. Ovplyvňuje sa soľný roztok ditioničitanV dôsledku toho sa pomocou chloridu amónneho kov zráža už vo forme fremy soli. Zrazenina sa premyje, filtruje a kalcinuje. Výsledkom všetkých týchto akcií je huby osmium. Následne sa vyčistí pomocou kyselín, obnoví sa v elektrickej peci pod prúdom vodíka a ochladí sa. tak dostanú vzorky osmium až do 99,9%.


chemický
Vlastnosti tohto prvku z hľadiska chémie sú úžasné. Nasledujúce sa považujú za najzákladnejšie z nich.
- Osmium vôbec nereaguje s alkáliami a kyselinami. Vytvára vo vode rozpustné osmata v reakcii s alkalickými topeniami. Interakcia so zmesou kyseliny dusičnej a kyseliny chlorovodíkovej spôsobuje extrémne pomalú reakciu.
- Veľmi jedovatý, dokonca aj pri mikroskopických dávkach. Obzvlášť toxický je oxid osmičitý uvoľňovaný z platiny.
- Nie je možné určiť teplotu varu kovu, pretože je zvlášť žiaruvzdorný.
- Kov v prášku ľahko reaguje s nasledujúcimi látkami: čistý kyslík, halogény, kyselina sírová alebo kyselina dusičná.
- V rôznych zlúčeninách dostáva oxidové čísla od -2 do +8. Najbežnejšie sú +2, +3, +4 a +8.
- Schopné tvoriť klastrové zlúčeniny.
- Hlavné minerály súvisia s tuhými roztokmi a sú zastúpené zliatinami irídia s osmium - sú to sysertskit a nevyanskit. Okrem toho má syrskit odlišné meno - iridium osmium a nevyanskite - osmisty iridium.

fyzický
hustota Osmium je približne 22,61 gramov na kubický centimeter. Kryštály majú krásny strieborný lesk s rôznymi odtieňmi od šedej po modrú. Ingoty majú tmavo modrú farbu v práškovej fialovej farbe. Celý kov má strieborný lesk. Toxicita prvku neumožňuje jeho použitie v klenotníckom priemysle. Hlavné fyzikálne vlastnosti sú také známe.
- Teplota topenia tohto prvku je pomerne vysoká, topenie je možné pri teplote vyššej ako 3 000 stupňov Celzia.
- Kov nemá žiadne magnetické vlastnosti.
- Úžasná tvrdosť. Zliatiny s pridaním tohto kovu získavajú zvýšenú odolnosť proti opotrebeniu, trvanlivosť, antikoróznu odolnosť a odolnosť voči mechanickému namáhaniu.
- Teplota varu je 5012 ° C.
- Mohsova tvrdosť je 7.
- Tvrdosť podľa Vickersa je 3-4 GPa.

Oblasti použitia
Z dôvodu značných nákladov na samotný prvok sa tento kov zriedka používa v hromadnej priemyselnej výrobe. Rozsah pôsobnosti osmium predstavuje najmä priemysel v chemickom priemysle, kde sa používa ako katalyzátor. Oxid osmičelý sa používa ako súčasť niektorých liekov. V laboratórnych testoch sa používa na farbenie živých tkanív, zaisťuje zachovanie bunkovej štruktúry.
V leteckom priemysle sa používa osmium v elektronickom vybavení zariadení pre leteckú a raketovú techniku, ako aj vo výrobe jadrové zbrane. Kvôli nedostatku magnetických vlastností kov sa používa na výrobu značkových hodiniek, napríklad Rolex. Používa sa zliatina osmium s platinou vytváranie chirurgických implantátov - Jedná sa o kardiostimulátory alebo pľúcne kufrové ventily.
Okrem toho sa osmium používa v mikroskopii a na vytváranie vysoko presných zariadení.



Zaujímavé fakty
- Osmium pri tlaku asi 770 GPa interaguje s elektrónmi vo vnútorných obežných dráhach, štruktúra látky zostáva nezmenená.
- kovový prvok v horninách obsahuje pol percenta z celkovej hmotnosti ložísk rúd.
- Kvôli vysokej hustote Vzhľad a skutočná hmotnosť kovu sú veľmi odlišné. 0,5-litrová plastová fľaša naplnená týmto kovovým práškom bude ťažšia ako 10-litrová vedra naplnená vodou.
- Tento kov je medzi prvými piatimi nákladný.
- Náklady na trojnásobnú uncu osmium sú obchodným tajomstvom, v otvorených zdrojoch nájdete približnú cenu za 1 gram látky.
- Kvôli žiaruvzdornosti osmium zaznamenané v histórii elektrickej lampy. Vedec K. Auer von Welsbach z Nemecka navrhol nahradiť vlákno osmium v uhoľnej žiarovke. Žiarovky sa ukázali byť 3 krát menej náročné na energiu a osvetlenie sa výrazne zlepšilo. Je pravda, že ho čoskoro nahradilo bežnejšie tantal, ktoré bolo nahradené volfrámom.
- Podobná situácia nastala pri výrobe vzácnych kovov a pri výrobe amoniaku. Metóda syntézy amoniaku, ktorá sa v súčasnosti používa, ktorú vyvinula v roku 1908 chemik Fritz Haber z Nemecka, je bez použitia katalyzátorov nemožná.Katalyzátory použité v tom čase spočiatku vykazovali svoje vlastnosti iba v prítomnosti významných teplotných podmienok a nemali vysokú účinnosť, takže hľadanie náhrady bolo veľmi relevantné. Vedci z laboratória Vyššej technickej školy v Karlsruhe navrhli použitie jemne rozptýleného osmia vo forme katalytického prvku. Výsledky testov potvrdili, že táto myšlienka bola užitočná, katalytická teplota sa znížila o viac ako 100 ° C a výstup amoniaku sa výrazne zvýšil. Je pravda, že v budúcnosti odmietali osmium, ale pomohol vyriešiť taký dôležitý problém.

Hrá sa osmium a ďalšie vzácne a jedinečné kovy významnú úlohu v rôznych priemyselných odvetviach, Aj napriek všetkej jej toxicite zachraňuje životy a zdravie ľudí.
Viac informácií o osmiume nájdete v nasledujúcom videu.










