ozmium - egy ritka fém, a platina csoportba tartozik. Ezt Angliában fedezték fel a platina reakciójának kísérletei eredményeként. Az osmium nevet görögül adják, és fordításában „szagot” jelent. Mi ez a nemesfém? Milyen tulajdonságai vannak, és mi a felhasználása?

A történet
Ennek az elemnek a felfedezése véletlenszerűen történt 1803-ban, a brit vegyészek Smithson Tennant és William H. Wallastan által. A platina és a savak (kénsav és salétromsav) keverékével történő reakciójának kísérlete eredményeként a kapott csapadék kellemetlen aromát mutatott, amely a klór és a rothadt retek szagára emlékeztetett. Hasonló kísérleteket végzett Colle Descotti, Antoine de Fourcoy és Vauclins Franciaországban. Kutatásaik eredményeként ismeretlen anyagot is találtak a platina oldhatatlan csapadékában.



Az ismeretlen anyagot ezután pten néven kapta, de a brit kísérletek bebizonyították, hogy ezek két hasonló anyag - irídium és ozmium.
Ezen kémiai elemek felfedezését a londoni Királyi Társaság elé terjesztették a Tennant által, 1804. június 21-én írt írásbeli üzenettel. A kémiai elemek periódusos táblájában a fém a 76 sorszám alatt helyezkedik el. A fémet tiszta formájában nem találják meg a rögök, ezért kémiai összetételét oldott formában mutatják be.


Az elembányászat újrahasznosított anyagokból készül. az irídium, platina, platina-palládium érc, réz és nikkel ércek elválasztása eredményeként. A teljes elem éves termelése a világon nem haladja meg az 1 tonnát.


letét
Érdemes megjegyezni a világ legnagyobb betéteit Urál-hegység és Szibéria Oroszországban, az északi államban Alaszka és a nyugati állam Kalifornia Amerikában Kanada Észak-Amerikában Colombia Dél-Amerikában és néhányban Dél-afrikai országok, AusztráliaA sziget Tasmania. Jelenleg fontolóra veszik az ozmium jelentős lerakódását Bushel komplexum Dél-Afrikában, ott kapják a legtöbb cuccot. Tekintettel arra, hogy a legnagyobb fémlerakódások Dél-Afrikában vannak, ennek a ritkaföldfémnek a világpiaci ára meglehetősen magas. Kazahsztán A világon az ozmium-187 egyetlen legnagyobb exportőre. Habár Kína rendelkezik platinaérctartalékokkal, nincs jelentős mennyiségű ozmium.


Az anyagot por formájában tárolják, és mivel nem olvad kristályok formájában, fizikai tulajdonságai miatt nem lehet jelet rárakni. Ennek a fémnek a rúdjai előállításához porból elektronnyalábot vagy ívhevítést használnak, valamint egy tégelyben történő melegítést is használnak.


A tulajdonságok
Az Osmium ezüstkék fémből néz ki. Ez az egyik legsűrűbb elem, sűrűsége 22 600 kilogramm / köbméter, de ugyanakkor az anyag meglehetősen törékeny, könnyen elbomlik és összeomlik. Magas fajsúlya és még meglehetősen magas hőmérsékleti behatások esetén is képes ragyogni. A paraméterek és a jelentős olvadási hőmérséklet miatt nehéz megmunkálni. A természetben hét izotóp formájában létezik, amelyek közül hatot stabilnak tekintnek: ozmium-184, ozmium-187, ozmium-188, ozmium-189, ozmium-190 és ozmium-192. A 162 és 197 tömegszámú radioaktív fém izotópokat laboratóriumi úton állították elő, és néhány nukleáris izomert szintén mesterségesen nyertek.
Jellemzői szerint az ozmium hátrányosan érinti az összes élő szervezetet.

Szinte az összes ilyen fémet tartalmazó vegyület károsítja a belső szerveket, látási, hallási rendellenességeket. Ozmium-párok általi mérgezés esetén a szervezetben visszafordíthatatlan rendellenességek és halál léphet fel. A tudósok állatokon végeztek kísérleteket, amelyek eredményeként a vérszegénység gyors fejlődése és a normál tüdőfunkció hiánya volt. Megállapítottuk, hogy ez egy gyorsan fejlődő ödéma. Az orvostudományban használt ozmium-tetraoxid nagyon agresszív anyag. Illata a legrosszabb a illata a világon. Mérgezéskor a bőr szenved, zöldre vagy feketére változik, gyakran fekélyekkel és repedésekkel jár, amelyek gyógyulása nagyon hosszú időbe telik.

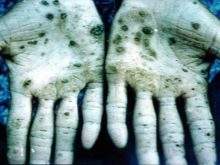

Az ipari helyiség alkalmazottai vannak a legnagyobb veszélyben, minden biztonsági előírás szerint csak légzőkészülékben és speciális ruházatban dolgoznak. Az összes ozmium-oxidot tartalmazó tartályt lezárják és a szabályoknak megfelelően tárolják. A Nevyanskite ásványok előállításához a platint aqua regia segítségével oldatká alakítják. Ezután a képződött csapadékot nyolcszoros mennyiségű cinkkel kezeljük - ez az ötvözet viszonylag könnyen por alakúvá alakul, amelyet ezután bárium-peroxiddal olvadunk. A következő lépés a kapott tömeg feldolgozása aqua regia alkalmazásával, desztillációval az ozmium-tetroxid elválasztására szolgáló berendezésen keresztül.

Az anyag lúgos oldatnak való kitettségével sót kapunk. A sóoldat befolyásolja hiposzulfitEnnek eredményeként ammónium-klorid segítségével a fém már Fremy-só formájában kicsapódik. A csapadékot mossuk, szűrjük és kalcináljuk. Mindezen műveletek eredménye szivacsos ozmium. Ezt követően savakkal megtisztítják, hidrogénáram alatt elektromos kemencében visszaállítják és lehűtik. így akár 99,9% -os osmiummintákat kaphat.


vegyi
Ennek az elemnek a tulajdonságai a kémia szempontjából csodálatosak. A következők tekinthetők legalapvetőbbnek.
- Az ozmium egyáltalán nem reagál lúgokkal és savakkal. Vízben oldódó osmát képez lúgos olvadékkal reagálva. A salétromsav és sósav keverékével való kölcsönhatás rendkívül lassú reakciót eredményez.
- Nagyon mérgező, még mikroszkopikus dózisokban is. Különösen mérgező a platinból felszabaduló ozmium-oxid.
- Lehetetlen meghatározni a fém forráspontját, mivel ez különösen tűzálló.
- A porban lévő fém könnyen reagál a következő anyagokkal: tiszta oxigén, halogén, kénsav vagy salétromsav.
- Különböző vegyületekben az oxidszáma -2 és +8 között van. A leggyakoribb +2, +3, +4 és +8.
- Képesek klasztervegyületek kialakítására.
- A fő ásványok szilárd oldatokhoz kapcsolódnak, és az irídium ötvözete ötvözi az ozmiummal - ezek sysertskite és nevyanskite. Ezenkívül a syrskite más néven szerepel - iridium osmium és a nevyanskite - osmicy iridium.

fizikai
sűrűség Az ozmium körülbelül 22,61 gramm / cm3. A kristályok gyönyörű ezüst színűek, különféle árnyalatokkal szürkétől kékig. A rúd sötétkék színű, a por ibolya. Az összes fém ezüstös fénye van. Az elem toxicitása nem teszi lehetővé az ékszeriparban történő felhasználását. A fő fizikai tulajdonságok ilyenek.
- Ennek az elemnek az olvadáspontja meglehetősen magas, az olvadás 3000 Celsius foknál magasabb hőmérsékleten lehetséges.
- A fémnek nincs mágneses tulajdonsága.
- Csodálatos keménység. Az ötvözetek ezen fém hozzáadásával megnövelik a kopásállóságot, a tartósságot, a korróziógátló hatást és a mechanikai igénybevételnek való ellenállást.
- A forráspont 5012 ºC.
- A Mohs keménysége 7.
- A Vickers keménysége 3-4 GPa.

Alkalmazási területek
Maga az elem jelentős költségei miatt ezt a fémet ritkán használják a tömeggyártásban. Az ozmium hatókörét elsősorban az ipar képviseli a vegyiparban, ahol katalizátorként használják. Az ozmium-tetraoxidot egyes gyógyszerek részeként használják. Laboratóriumi vizsgálatok során élő szövetek festésére használják, biztosítja a sejtszerkezet megőrzését.
A repülőgépiparban az ozmiumot használják repülési és rakétatechnikai berendezések elektronikus berendezéseiben, valamint a gyártásban nukleáris fegyverek. A mágneses tulajdonságok hiánya miatt A fémet márkás órák, például Rolex gyártásában használják. Az ozmium és a platina ötvözetét használják műtéti implantátumok készítése - Ezek szívritmus-szabályozók vagy tüdőérzékelő szelepek.
Ezenkívül az ozmiumot használják a mikroszkópiában és a nagy pontosságú eszközök létrehozásához.



Érdekes tények
- Körülbelül 770 GPa nyomáson az ozmium kölcsönhatásba lép az elektronokkal a belső pályákon, az anyag szerkezete változatlan marad.
- ozmium a kőzetekben az érclerakódások teljes tömegének fél százalékát tartalmazza.
- A nagy sűrűség miatt a fém megjelenése és tényleges tömege nagyon különböző. Tehát egy 0,5 literes műanyag palack, amely ezzel a fémporral van feltöltve, nehezebb lesz, mint egy 10 literes vödör.
- Ez a fém az első ötben van drága.
- Az ozmium hármas uncia ára üzleti titok, a nyílt forrásokban megtalálja az 1 gramm anyag hozzávetőleges árat.
- Az ozmium fénytörő képessége miatt megjegyezte az elektromos lámpa történetében. A német K. Auer von Welsbach tudós javaslatot tett a szénhagymában lévő ozmium rost helyettesítésére. Az izzók háromszor kevésbé energiaigényesek, és a világítás jelentősen javult. Igaz, hamarosan helyette a közönséges tantál váltotta fel, amelyet viszont a volfrám váltott fel.
- Hasonló helyzet történt a ritka fémekkel és az ammónia előállításával. A jelenleg alkalmazott ammóniaszintézis módszer, amelyet 1908-ban fejlesztett ki a német Fritz Haber vegyész, katalizátorok használata nélkül lehetetlen.Az eredetileg alkalmazott katalizátorok kezdetben csak jelentős hőmérsékleti viszonyok mellett mutatták meg tulajdonságaikat, és nem voltak nagy hatékonyságuk, tehát a cserekeresés nagyon releváns volt. A karlsruhei Felső Műszaki Iskola laboratóriumának tudósai javaslatot tettek a finoman diszpergált ozmium katalitikus elem formájában történő felhasználására. A teszteredmények megerősítették, hogy ez az ötlet érdemes, a katalitikus hőmérséklet több mint 100 ºC-kal csökkent, és az ammóniakibocsátás jelentősen megnőtt. Igaz, később megtagadták az ozmiumot, de ez segített egy ilyen fontos probléma megoldásában.

Az ozmium és más ritka és egyedi fémek játszanak jelentős szerep a különféle iparágakban. Még minden toxicitása mellett megmenti az emberek életét és egészségét.
További információt az ozmiumról a következő videóban találhat.










