osmijum - rijedak metal, pripada skupini platina. Otkrivena je u Engleskoj kao rezultat pokusa na reakciji platine. Naziv osmij dat je na grčkom jeziku i u prijevodu znači "miris". Što je ovaj plemeniti metal? Koje su njegove karakteristike i u čemu se koristi?

Priča
Otkrivanje ovog elementa dogodilo se slučajno 1803. godine od strane britanskih kemičara Smithsona Tennanta i Williama H. Wallastana. Kao rezultat pokusa reakcije platine na mješavinu kiselina (sumporne i dušične), rezultirajući talog pokazao je neugodnu aromu koja podsjeća na smrad klora i trule rotkvice. Slične su eksperimente izveli Colle Descotti, Antoine de Fourcoy i Vauclins u Francuskoj. Kao rezultat svojih istraživanja, također su pronašli nepoznatu tvar u netopljivom talogu iz platine.



Tada je nepoznata tvar dobila ime pten, ali britanski su pokusi dokazali da su to dvije slične tvari - iridium i osmium.
Otkriće tih kemijskih elemenata predstavljeno je Kraljevskom društvu u Londonu pisanom porukom Tennanta od 21. lipnja 1804. U periodnoj tablici kemijskih elemenata metal se nalazi pod rednim brojem 76. Naggets ne pronalazi metal u svom čistom obliku, stoga je njegova kemijska formula predstavljena u otopljenom obliku.


Rudanje elemenata je iz recikliranih materijala. kao rezultat njegovog odvajanja od ruda iridija, platine, platine i paladija ili ruda bakra i nikla. Godišnja proizvodnja cjelokupnog elementa u svijetu ne prelazi veličinu od 1 tone.


depozit
Najveća svjetska ležišta vrijede spomenuti i takva područja kao Uralske planine i Sibir u Rusiji, sjevernoj državi Aljaska i zapadne države Kalifornija u Americi Kanada u Sjevernoj Americi Kolumbija u Južnoj Americi i neke Južnoafričke države, AustralijaOtok Tasmanija, Trenutno se razmatra značajno ležište osmija Bushel kompleks u Južnoj Africi, tamo dobivaju najviše stvari. S obzirom na to da su najveća ležišta metala u Južnoj Africi, svjetske cijene za taj rijetkozemni metal su prilično visoke. Kazahstan Smatra se jedinim najvećim izvoznikom osmija-187 na svijetu. Iako Kina ima rezerve platinske rude, ona nema značajnu količinu osmija.


Tvar se skladišti u praškastom obliku, a budući da se ne topi u obliku kristala, na fizička svojstva nije moguće staviti oznaku. Za proizvodnju ingota ovog metala koristi se elektronsko zračenje ili lučno grijanje iz praha, a koristi se i grijanje u loncu.


Svojstva
Osmium izgleda kao srebrno plavi metal. Ovo je jedan od najgušćih elemenata, njegova gustoća iznosi 22.600 kilograma po kubičnom metru, ali istodobno je tvar prilično krhka, lako se lomi i drobi. Ima visoku specifičnu težinu i može sijati čak i pri prilično visokim utjecajima temperature. Zbog parametara i značajne temperature taljenja, teško je obraditi. U prirodi postoji u obliku sedam izotopa, od kojih se šest smatra stabilnim, to su osmij-184, osmij-187, osmijum-188, osmijum-189, osmijum-190 i osmij-192. Radioaktivni metalni izotopi s masovnim brojem od 162 do 197 dobiveni su laboratorijski, a neki su nuklearni izomeri i umjetno dobiveni.
Osmij u svojim karakteristikama nepovoljno utječe na sve žive organizme.

Gotovo svi spojevi s ovim metalom uzrokuju oštećenja unutarnjih organa, vida, slušne poremećaje. U slučaju trovanja osmijskim parovima mogu se dogoditi nepovratni poremećaji u tijelu i smrt. Znanstvenici su provodili eksperimente na životinjama, čiji su rezultati bili brzi razvoj anemije, nedostatak normalne plućne funkcije. Zaključeno je da se radi o edemu koji se brzo razvija. Osmijev tetraoksid, koji se koristi u medicini, vrlo je agresivna tvar. Ima najgiblji miris na svijetu. Kod trovanja koža pati, mijenja boju u zelenu ili crnu, često je to popraćeno čirima i pukotinama koje će trebati vrlo dugo zacjeljivanje.

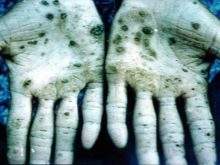

U najvećem su riziku zaposlenici industrijskih prostorija, a prema svim sigurnosnim standardima rade samo na respiratorima i u posebnoj odjeći. Svi spremnici koji sadrže osmijum oksid se hermetički zatvaraju i čuvaju u skladu s propisima. Da bi se dobili nevinjanski minerali, platina se pretvara u otopinu pomoću aqua regia. Zatim se dobiveni talog obrađuje s cinkom u 8-puta većoj količini - ta se legura relativno lako pretvara u stanje praha, koji se zatim stapa s barijevim peroksidom. Sljedeći korak je obrada rezultirajuće mase pomoću aqua regia, destilacija kroz aparat za odvajanje osmijum tetroksida.

Izlaganjem tvari alkalnoj otopini dobiva se sol. Utječe solna otopina hyposulfiteKao rezultat toga, uz pomoć amonijevog klorida, metalni talog se taloži već u obliku fremy-jeve soli. Talog se ispere, filtrira i kalcinira. Rezultat svih tih radnji je spužvasti osmij. Nakon toga se očisti kiselinama, obnovi u električnoj peći pod strujom vodika i ohladi. tako primaju uzorke osmija do 99,9%.


kemijski
S gledišta kemije svojstva ovog elementa su nevjerojatna. Sljedeće se smatra najosnovnijim od njih.
- Osmij uopće ne reagira s alkalijama i kiselinama. Tvori u vodi topivi osmata u reakciji s alkalnim talinama. Interakcija s mješavinom dušične i klorovodične kiseline daje izuzetno sporu reakciju.
- Vrlo otrovno, čak i u mikroskopskim dozama. Posebno je toksičan osmijum oksid koji se oslobađa iz platine.
- Nemoguće je odrediti temperaturu vrenja metala, jer je ona posebno vatrostalna.
- Metal u prahu lako reagira sa sljedećim tvarima: čistim kisikom, halogenima, sumpornom ili dušičnom kiselinom.
- U raznim spojevima dobiva oksidne brojeve od -2 do +8. Najčešći su +2, +3, +4 i +8.
- Sposoban je za stvaranje klasterskih spojeva.
- Glavni minerali odnose se na krute otopine i predstavljeni su legurama iridija s osmijem - to su sysertskite i nevyanskite. Štoviše, syrskite ima različit naziv - iridium osmium, a nevyanskite - osmisty iridium.

fizička
gustoća Osmij je otprilike 22,61 grama po kubnom centimetru. Kristali imaju prekrasan srebrnast sjaj, s raznim nijansama od sive do plave boje. Ingoti pokazuju tamno plavu boju, u praškastoj boji. Sav metal ima srebrnast sjaj. Toksičnost elementa ne dopušta njegovu upotrebu u industriji nakita. Primjećuju se glavna fizička svojstva.
- Talište ovog elementa je prilično veliko, taljenje je moguće pri temperaturi većoj od 3000 Celzijevih stupnjeva.
- Metal nema magnetska svojstva.
- Nevjerojatna tvrdoća. Legure s dodatkom ovog metala stječu povećanu otpornost na habanje, izdržljivost, antikorozijsku i otpornost na mehanički stres.
- Vrelište je 5012 ºC.
- Mohsova tvrdoća je 7.
- Vickersova tvrdoća je 3-4 GPa.

Područja primjene
Zbog značajnih troškova samog elementa, ovaj se metal rijetko koristi u masovnoj industrijskoj proizvodnji. Opseg osmija uglavnom predstavlja industrija u kemijskoj industriji, gdje se koristi kao katalizator. Osmijev tetraoksid koristi se kao dio nekih lijekova. U laboratorijskim testovima koristi se za bojenje živih tkiva, osigurava očuvanje stanične strukture.
U zrakoplovnoj industriji koristi se osmij u elektroničkoj opremi opreme za zrakoplovnu i raketnu tehnologiju, tako i u proizvodnji nuklearno oružje. Zbog nedostatka magnetskih svojstava, metal se koristi u proizvodnji markiranih satova kao što je Rolex. Za to se koristi legura osmija s platinom stvarajući kirurške implantate - To su pejsmejkeri ili plućni ventili debla.
Osim toga, osmij se koristi u mikroskopiji i za stvaranje visoko preciznih uređaja.



Zanimljive činjenice
- Pri tlaku od oko 770 GPa, osmij stupa u interakciju s elektronima u unutarnjim orbitalima, struktura tvari ostaje nepromijenjena.
- osmijum u stijenama sadrži pola posto ukupne mase ležišta rude.
- Zbog velike gustoće izgled i stvarna masa metala vrlo su različiti. Dakle, 0,5-litrena plastična boca napunjena ovim metalnim prahom bit će teža od kante od 10 litara napunjene vodom.
- Ovaj metal je u prvih pet skup.
- Cijena trostruke unce osmija je poslovna tajna, u otvorenim izvorima možete pronaći približnu cijenu za 1 gram tvari.
- Zbog vatrostalnosti osmija zabilježeno u povijesti električne svjetiljke. Znanstvenik K. Auer von Welsbach iz Njemačke predložio je zamjenu filamenta osmija u žarulji ugljena. Pokazalo se da su žarulje 3 puta manje energetske, a osvjetljenje se značajno poboljšalo. Istina, ubrzo ga je zamijenio uobičajenijim tantalom, koji je zauzvrat zamijenjen volframom.
- Slična se situacija dogodila s rijetkim metalima i u proizvodnji amonijaka. Trenutno korištena metoda sinteze amonijaka, koju je 1908. godine razvio kemičar Fritz Haber iz Njemačke, nemoguća je bez upotrebe katalizatora.U početku su tada korišteni katalizatori pokazali svoja svojstva samo u prisutnosti značajnih temperaturnih uvjeta i nisu imali visoku učinkovitost, pa je potraga za nadomjestkom bila vrlo relevantna. Znanstvenici iz laboratorija Više tehničke škole u Karlsruheu predložili su upotrebu fino dispergiranog osmija u obliku katalitičkog elementa. Rezultati ispitivanja potvrdili su da se ova ideja isplati, katalitička temperatura smanjila se za više od 100 ºC, a proizvodnja amonijaka značajno se povećala. Istina, kasnije su odbili osmij, ali to je pomoglo u rješavanju tako važnog problema.

Osmij i drugi rijetki i jedinstveni metali igraju značajnu ulogu u raznim industrijama, Čak i uz svu toksičnost, spašava život i zdravlje ljudi.
Više informacija o osmiju možete dobiti u sljedećem videu.










